
RSS-Feed der Bay. Landesanstalt für Wald und Forstwirtschaft abonnieren
So verpassen Sie keine Neuigkeiten mehr. Unser RSS-Feed "Nachrichten der Bayerischen Landesanstalt für Wald und Forstwirtschaft" informiert Sie kostenlos über unsere aktuellen Beiträge.
Eric Andreas Thurm, Wolfgang Falk und Stefan Müller-Kroehling
Die Flatterulme als Alternative bei der Baumartenwahl: Standorts- und Leistungspotenzial – LWF Wissen 83
Die Flatterulme (Ulmus laevis Pall.) weist als einzige europäische Art sehr regelmäßig kräftig entwickelte Brettwurzeln auf (siehe Abbildung 1), die an Baumarten der Tropenwälder erinnern. Auch Bergulme und Schwarzpappeln können recht ausgeprägte Brettwurzeln aufweisen, doch wesentlich seltener und auch weniger stark ausgeprägt in den Dimensionen.
Die Brettwurzeln haben die Funktion, die Standfestigkeit der Bäume auf ganzjährig vernässten Standorten zu verbessern. Die Flatterulme bildet diese Eigenschaft jedoch auch auf trockneren Standorten aus, wenn auch meist weniger stark ausgeprägt. Dies ist ein Indiz, dass im Laufe vieler Baumgenerationen eine Anpassung an vernässte Standorte erfolgt ist (Roloff 2010).
 Zoombild vorhanden
Zoombild vorhanden
Abb. 1: Brettwurzeln am Stammanlauf der Flatterulme kennzeichnen sie als Baumart der feuchten Standorte. (Foto: E. Thurm)
Trotz einiger sehr markanter Eigenschaften, wie eben die der Brettwurzeln, wurde sie als Art oft übersehen, in ihren Eigenschaften verkannt und sowohl in Forst als auch Landespflege weitgehend ignoriert (Müller-Kroehling 2003b). Bestandsweise Anbauten als führende Baumart wie jener in der Eichhorst bei Ratzeburg (Schmitz 1992) sind selten, und ergaben sich in diesem Fall auch durch eine Verwechslung bei der Beerntung mit der eigentlich angestrebten Feldulme (Schmitz, mdl. Mitt. Juli 2004).
Da neben verbreiteten Fehlbestimmungen oft in Erhebungen ohnehin nur die Gattung »Ulme« aufgenommen und nicht weiter differenziert wurde, ist sehr wenig über die forstlichen Kenngrößen dieser Art bekannt. Neben ihren Standortsansprüchen und ihrer Eignung im Klimawandel wollen wir in diesem Beitrag daher auch eine Einschätzung zum forstlichen Leistungspotenzial dieser heimischen Waldbaumart versuchen.
Ansprüche an Boden und Standort
 Zoombild vorhanden
Zoombild vorhanden
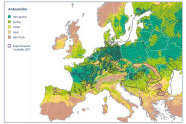
Abb. 2: Heutiges Anbaurisiko der Flatterulme in Europa basierend auf Inventurpunkten (schwarze Punkte) und einer Arealkarte (gleichmäßig verteilte schwarze Punkte) von Caudullo et al. (2017, blaue Linie). (Grafik: LWF)
Dennoch scheint sie auch in weniger feuchten Eichen-Hainbuchenwäldern als Mischbaumart geeignet zu sein. Zähe, plastische Standorte wie Tone und strenge Pseudogleye, wie sie für Eichen-Hainbuchenwälder typisch sind, stellen für die Flatterulme in der Regel kein Durchwurzelungshindernis dar (Köstler et al. 1968). Allerdings sind geopyhtenreiche Eichen-Hainbuchenwälder oft mangels Überflutung weniger empfänglich für die Naturverjüngung der Art (Dister 1980).
Auch wenn die Flatterulme typischer Weise auf frischen oder feuchten Standorten zu finden ist, erträgt sie doch auch Trockenheit aufgrund ihres ausgesprochen tief reichenden Wurzelwerkes (Köstler et al. 1968) gut, und ist auch für weniger feuchte, aber tiefgründig durchwurzelbare Böden geeignet und beispielsweise gegenüber abgesenktem Grundwasser weniger empfindlich (Vyskot 1984). Daher ist sie nicht nur in der Hartholzaue, sondern auch in eichenreichen Laubmischwäldern als Beimischung vorhanden, bis hin zu Vorkommen in der Waldsteppe (Collin 2003).
Die Anpassung der Flatterulme an Feuchtstandorte unterscheidet sie von der der Bergulme (Ulmus glabra Huds.) und Feldulme (Ulmus minor Mill.). Zwar kann die Feldulme wie die Flatterulme auch in bis zu drei oder sogar viereinhalb Monaten überschwemmten Auwäldern vorkommen (Späth 1988, ETH Zürich 1995, Macher 2008 mit einer Übersicht über eine Mehrzahl von Arbeiten, Li et al. 2015), doch fehlt sie in Bruchwäldern im Gegensatz zur Flatterulme vollständig. Sie ist der Flatterulme in Bezug auf die Überschwemmungstoleranz unterlegen (Li et al. 2015).
Neben der schon genannten Ausbildung von Brettwurzeln, ist eine weitere Anpassung der Flatterulme ein sehr tief reichendes Wurzelsystem (Köstler et al. 1968). Brettwurzeln dienen neben der Stabilisierung auf nassen, weichen Substraten auch einem verbesserten, diffusionsbedingten Lufteintritt in den Holzkörper und verbessern so die Sauerstoffversorgung der Wurzeln (Härdtle et al. 2004). Ob sie wie die Schwarzerle (Alnus glutinosa (L.) Gaertn.), mit der sie gemeinsam in Bruchwäldern vorkommen kann, auch über weitere spezielle morphologische oder physiologische Anpassungen verfügt, ist nicht bekannt. Möglicherweise stellen ihr im Vergleich zu Feld- und Bergulme besonders breiter Splint oder aber auch ein relativer Reichtum an Lentizellen eine spezielle Anpassung an die nassen Bedingungen ihres typischen Lebensraumes dar. Eine solche vermehrte Bildung »hypertrophischer Lentizellen am Stammfuß unter anoxischen Bedingungen« durch manche Baumarten »verbessert die Aufnahme von Sauerstoff und teilweise auch die Abgabe gasförmiger Stoffwechselprodukte« (Leuschner und Ellenberg 2017, S. 704). Gleiches gilt für Ihren im Vergleich zu Berg- und Feldulme wesentlich größeren Gefäß-Anteil und deren radiale Anordnung (Kutschera und Lichtenegger 2013).
Berg- und Feldulme stellen insgesamt erheblich höhere Ansprüche an den Nährstoffgehalt des Bodens (Hempel und Wilhelm 1889, Ellenberg 1992) und sind insofern stärker als die Flatterulme »Edellaubbäume«. Gleichwohl sieht Kreutzer (1987) ihre »Hauptverbreitung auf nährstoffreichen Silikatstandorten«, und Sauter (2003) sie als Trennart für eine »Ulmus laevis-Gebietsausbildung « des »nährstoff- und stickstoffreichen Hartholzauwaldes Süddeutschlands«.
Ein weiterer Unterschied der Flatterulme zu den anderen beiden Ulmenarten und den Edellaubbäumen ist ihre mutmaßlich geringe und tatsächliche Kalktoleranz. Manche Auenbaumarten wie auch die Stieleiche (Quercus robur L.) leiden auf sehr kalkreichen Standorten unter einer milden Kalkchlorose, die sich durch die Festlegung von Eisen und Mangan in Komplexverbindungen erklärt, die bei hohen pH-Werten entstehen und für den Baum nicht nutzbar sind. Dieser Mangel macht sich durch hellgrüne Belaubung bemerkbar. Kreutzer (1987) reiht die Flatterulme unter den Baumarten mit »mäßiger Kalktoleranz«, auch wenn sie in den kalkhaltigen Auen nicht fehle, während sie nach ETH Zürich (1995) sogar ein »schwacher Kalkzeiger« sein soll. Seibert (1987) schreibt, dass sie »kalkreiche Standorte meide.«
Ihre Fähigkeit, sehr basenreiche Böden zu besiedeln, ist in der Tat geringer als bei Berg- und Feldulme, da das Aneignungsvermögen für Eisen und Mangan bei hohen pH-Werten weniger gut ausgeprägt ist als bei jenen (Venturas et al. 2014a). Dies könnte sich durch die fehlende Notwendigkeit, hierfür spezielle Aneigungsmechanismen zu entwickeln, erklären, da sie ja vorwiegend auf Feuchtstandorten vorkommt. Auf solchen Standorten mit Hydromorphie-Merkmalen, also allen Feuchtstandorten oder solchen mit Unterbodenfeuchte, geraten Eisen- und Mangan hinreichend in Lösung und können auch von weniger gut an kalkreiche Standorte angepassten Baumarten wie Stieleiche und eben Flatterulme ausreichend angeeignet werden. Kreutzer (1987) sieht eine »optimale Phosphaternährung« als wichtiges Merkmal guten Wachstums dieser Baumart an.
Dass alle drei Arten als »Ulmen« subsummiert und behandelt werden, auch in Baumarten-Eignungstabellen und anderen forstlichen Empfehlungen, ist aufgrund der sehr unterschiedlichen Ansprüche an und Toleranzen gegenüber Boden und Standort zusammenfassend weder sachgerecht noch hilfreich (Müller-Kroehling 2003).
Boden und Anbaurisiko – »Patch-Tabelle«
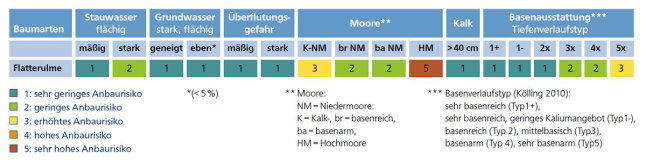
Eine Expertenbefragung in Verbindung mit Daten- und Literaturauswertungen bestätigt der Flatterulme ebenfalls die oben genannten geringen Einschränkungen auf schwierigen Standorten (Tabelle 1, Thurm und Falk 2019). Weder eine gerige Basenversorgung noch Einfluss von Stau- oder Grundwasser sind ein harter Ausschlussgrund, letzteres sogar im Gegenteil ein Konkurrenzvorteil. Lediglich auf dauernassen oder extrem nährstoffarmen Standorten wie Hochmooren, oder natürlich auf Trockenstandorten sind Flatterulmen fehl am Platz.
Klimatische Ansprüche
Vorkommen in Europa
In Bezug auf die Frostgefährdung ist zu erwähnen, dass die sehr früh im Jahr erscheinenden Blüten erfrieren können. ETH Zürich (1995) stuft sie für die Schweiz als unempfindlich gegen Spätfrost ein, erwähnt aber eine Empfindlichkeit gegenüber Frühfrösten und Frostrissen.
Artverbreitungsmodelle
Ein wichtiger Einsatzbereich dieser Modelle ist die Vorhersage von Auswirkungen einer Klimaerwärmung auf die Verbreitung von Arten. Nur sehr wenige Forstinventuren führen die Flatterulme überhaupt als eigene Art und subsumieren sie nicht unter ›Ulmen‹ oder ›andere Laubhölzer‹. Um dennoch eine Anbaurisikokarte für die Art zu generieren und somit einen Blick in die Zukunft wagen zu können, wurde die ökologische Nische der Flatterulme mithilfe (1) einer auf Expertenwissen basierenden Arealkarte von Caudullo et al. (2017) modelliert.
Über Europa wurde dazu ein gleichmäßiges Raster gelegt. Alle Punkte, die in diese Arealkarte fallen und sich innerhalb von Waldflächen (Kempeneers et al. 2011) befinden, dienten als Vorkommen (Präsenzen der Flatterulme). Punkte außerhalb der Arealkarte dienen als Nicht-Vorkommen (Absenzen). Der Datensatz wurde erweitert um Flatterulmen-Vorkommensdaten aus (2) einer Datensammlung seltener Baumarten aus Forstinventuren (Thurm et al. 2018) und aus (3) der Globalen Biodiversitätsdatenbank (GBIF.org 2019). Die Vorkommen aus den drei verschieden Datenquellen sind in Abbildung 2 dargestellt. Deutlich zu erkennen sind die gehäuften Vorkommen im Westen und Südosten Europas (GBIF. org und Inventurdaten) und die aus der Arealkarte per Raster ausgelesenen regelmäßigen Punkte im Osten.
Die ökologische Nische der Flatterulme wurde aufbauend auf diesen Daten durch ein generalisiertes additives Modell (GAM) modelliert. Als Umweltvariablen wurde die Mitteltemperatur im Sommer, im Winter (Klimadaten aus Fick und Hijmans 2017) und den Grad der Kontinentalität nach Conrad 1946 genutzt. Von diesen drei Variablen hatte die Sommertemperatur den größten Einfluss. Es wurden keine Niederschlagsvariable in dem Modell verwendet, da die Flatterulme natürlicher Weise, wie schon erwähnt, vor allem in Feuchtwäldern vorkommt. Sie wächst somit in den azonalen Vegetationen, welche sehr stark von extremen Bodenfaktoren, in diesem Fall Überflutung bzw. sehr hoher Grundwasserspiegel, geprägt sind (Ellenberg und Dierschke 2010). Der Niederschlag spielt also für die Verbreitung der Flatterulme zumindest auf diesen Standorten eine untergeordnete Rolle.
Klimahülle
 Zoombild vorhanden
Zoombild vorhanden
Abb. 3: Klimahülle der Flatterulme mit den Achsen
Jahresniederschlag und Jahresmitteltemperatur (Grafik: LWF)
Dabei sind die unterschiedlichen Datengrundlagen zu beachten: Stieleiche und Esche wurden mit dem Datensatz aus Thurm et al. 2018 erstellt, der sich aus Forstinventuren zusammensetzt und kaum Vorkommen aus Russland beinhaltet. Dennoch sind sowohl Esche als auch die Stieleiche hier noch vertreten (Caudullo et al. 2017). Dieser Effekt (nur bei einer von drei Arten Daten aus Russland) ist im kontinental kühlen und trockenen Ast der Klimahülle zu sehen: Die Hülle der Flatterulme reicht hier viel weiter. Der Unterschied in der Abbildung beruht also in diesem Klimabereich nicht primär auf unterschiedlichen Verbreitungen, sondern auf unterschiedlichen Datenquellen. Interessanter ist daher der Vergleich der übrigen Ränder der Klimahüllen.
Bezüglich der Wärme ist die Flatterulme bei niedrigen Niederschlagssummen etwas toleranter, die beiden anderen Arten hingegen bei gleichzeitig etwas höheren Niederschlagssummen (Niederschläge können höhere Temperaturen kompensieren). Dass die Flatterulme den anderen beiden Arten hier wenig nachsteht, ist etwas deutlicher zu sehen, wenn nicht allein die Hülle mit der Dichtefunktion, sondern zusätzlich die Boxplots neben den Achsen betrachtet werden: Hier sind Flatterulmenvorkommen bis zu Jahresdurchschnittstemperaturen von 15 °C zu erkennen. Grundsätzlich reicht die Verbreitung von Stieleiche und Esche allerdings etwas weiter in den Süden Europas (Caudullo et al. 2017).
Die drei Arten unterscheiden sich nur geringfügig bei der Trocken- und Wärmegrenze. Der Unterschied bei der Kältegrenze ist wie erläutert zum einen vermutlich von der Datengrundlage verursacht. Zum anderen ist die Flatterulme aber diejenige der drei Arten, deren Verbreitung am weitesten in den kontinentalen Osten Europas reicht und somit bezüglich Frosthärte und ggf. Spätfrösten die größte Toleranz hat. Einen weiteren deutlichen Unterschied gibt es bei der Verbreitungsgrenze hin zu höheren Niederschlägen, die in der Regel mit höheren Lagen einhergehen.
So ist die Esche beispielsweise in den Bayerischen Alpen bis 1.450 m zu finden, eine Höhenlage, die mit der Verbreitungsgrenze der Bergulme vergleichbar ist (Ewald und Kölling 2009). Schütt et al. (2002) geben für die Flatterulme eine Verbreitung im Gebirge von selten höher als 600 m an, für die Stieleiche in den Alpen bis 950 m und in Übereinstimmung mit Ewald und Kölling (2009) für die Esche in den Nordalpen 1.400 m. ETH Zürich (1995) nennt für die Schweiz 450 m und für Ungarn 630 m als Höhen-Verbreitungsgrenze der Flatterulme. Bei der Höhenverbreitung sollte jedoch auch berücksichtigt werden, dass sie eher eine Art sumpfiger Bereiche und des ufernahen Schwemmlandes ist, so dass sie in den höher gelegenen Auen auch stellenweise nicht die optimalen Standortsbedingungen vorfindet.
Dokumentierte Funde vitaler Flatterulmen in montanen Lagen lassen den Schluss zu, dass sie weder sehr wärmeliebend noch sehr frostempfindlich ist. Clauss (Müller-Kroehling und Clauss 2011) fand sie an einem Bachlauf im rauen Klima des Fichtelgebirges oberhalb 600 NN, Degenhard (2016) in einem Fichten-Buchen- Mischbestand östlich Kaufbeuren bei über 750 m NN.
Aktuelle und zukünftig mögliche Verbreitung in Bayern
 Zoombild vorhanden
Zoombild vorhanden
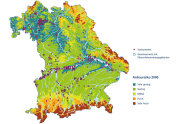
Abb. 4: Anbaurisiko bezüglich Temperaturen für die Flatterulme im Zeitraum 1970–2000. (Grafik: LWF)
In der Abbildung hinterlegt ist das oben beschriebene Artverbreitungsmodell mit dem Farbcode aus dem Bayerischen Standortinformationssystem BaSIS (Taeger und Kölling 2016): Dunkelgrün bedeutet ein sehr geringes, rot ein sehr hohes Anbaurisiko. Da das Modell auf vor allem auf der Sommertemperatur beruht, sind besonders die kühlen Hochlagen zu erkennen. Sie haben ein hohes Anbaurisiko. Umgekehrt ist das Anbaurisiko in den wärmeren Tieflagen gering. Das hinterlegte Modell zeigt: Die meisten Vorkommen liegen in den grün klassifizierten Regionen, nur wenige Einzelvorkommen sind in aufgrund der Temperaturen gelb oder orange eingestuft werden.
 Zoombild vorhanden
Zoombild vorhanden
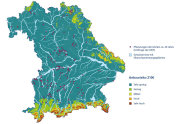
Abb. 5: Anbaurisiko bezüglich Temperaturen für die Flatterulme im Zeitraum 2070–2100. (Grafik: LWF)
Eine Abfrage bei den bayerischen Ämtern für Ernährung, Landwirtschaft und Forsten (AELF) und den Bayerischen Staatsforsten (BaySF) zu Pflanzungen von Flatterulmen in den letzten Jahren ergab, dass sie ausnahmslos in Gebieten erfolgt sind, die derzeit schon geeignet und bei einer moderaten Temperaturerhöhung zum Teil sogar noch besser geeignet sind, die Baumartenwahl also vorausschauend erfolgte. Diese Pflanzungen mit der Flatterulme sind also eine Ergänzung des Baumartenspektrums in Bayern mit einer heimischen Baumart, die mit höheren Temperaturen und zugleich schwierigen Standorten zurechtkommt.
Leistung
 Zoombild vorhanden
Zoombild vorhanden
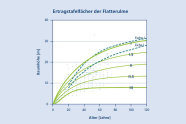
Abb. 6: Ertragstafelfächer der Flatterulme, basierend auf Forstinventurdaten von Bäumen der Kraft’schen Klasse I und II (durchgezogene Linien). (Grafik: LWF)
Dennoch sind in den heimischen Wäldern immer wieder Exemplare zu finden, die bis zu 35 m erreichen können, vor allem auf tiefgründigen, weniger extremen Standorten, die man ihr sonst oft nicht zugestanden hat. Bestände mit führender Flatterulme beispielsweise in Mischung mit Stieleiche und Esche oder Schwarzerle existieren und sind ohne großen Pflegeaufwand möglich, da die Flatterulme durchaus konkurrenzkräftig sein kann. Auch in durchaus wüchsigen Fichtenbeständen in der Aue kann sie sich zum Teil ohne jede Förderung behaupten (Müller-Kroehling unveröff. 1999 in der Isaraue bei Oberhummel; Degenhardt 2016 für das Gebiet zwischen Isar und Lech).
Sie ist schattentoleranter als die Feldulme (Prpic et al. 2005) und wird von diesen Autoren als Halbschattbaumart charakterisiert. Für diese Einstufung sprechen auch die mehrschichten Bestände von Flatterulme und Schwarzerle an der Amper ebenso wie die von der Flatterulme aus Naturverjüngung gebildete zweite Baumschicht in den feuchten Eichen- Hainbuchenwäldern des Davert südlich Münster (Müller-Kroehling, unveröff.). Auch der Blattflächenindex von 5.4 (Jaro 1959 in Leuschner und Ellenberg 2017) liegt höher als bei den reinen Lichtbaumarten, aber niedriger als bei den Schattbaumarten.
Welche wachstumskundliche Grundlage diese Zusammenfassung der Ulmen mit den Eichen bzw. Eschen hat, ist zwar nicht näher bekannt, alle drei Baumarten gehören jedenfalls zu den ringporigen Laubhölzern und besetzen vergleichbar den Standort der Hartholzaue. Die anatomischen und standörtlichen Ähnlichkeiten legen eine gewisse Vergleichbarkeit daher nahe. Für diesen Artikel wurde daher versucht, mit den obengenannten Inventurdaten (Thurm et al. 2018) einen Bonitätsfächer der Baumart (Brandl et al. 2018) aufzuspannen. Hiermit soll ein erster Eindruck gewonnen werden, wie sich das Höhenwachstum der Flatterulme gegenüber dem Wachstum von Eiche und Esche der Ertragstafel verhält (siehe Abbildung 6).
Eingegangen sind dazu Forsteinrichtungsdaten aus Bulgarien (N = 326), Ungarn (N = 137), Polen (N = 75) und Inventurdaten aus anderen EU-Staaten (N = 3). Es handelt sich dabei vornehmlich um Mittelhöhen des Oberstandes und um Einzelbaumdaten. Zwar sind nur Bäume der Kraft’schen Klasse 1 und 2 eingeflossen, dennoch zeigt die abgebildete Kurve eher einen Verlauf der Mittelhöhen als der Oberhöhen.
Die Flatterulme zeigt ein ähnlich zügiges Höhenwachstum in der Jugend wie die Esche. In der Ertragsklasse I, wird eine Mittelhöhe von etwa 29 m im Alter 100 erreicht. Es ist zu vermuten, dass in Europa klimatisch wahrscheinlich noch leistungsfähigere Standorte zu finden sind, die auch Bonitäten zwischen der 0 und der I. Ertragsklasse aufweisen. Mayer 1992 beschreibt beispielsweise die gutgeformten, wüchsigen Ulmen im ›baltischem Lehmrevier‹/Litauen. Sie ist also auf den entsprechenden Standorten keinesfalls eine »Baumart 2ter Ordnung«.
Der Vergleich der Ertragsklasse I von Esche und Eiche zur Flatterulme in Abbildung 6 zeigt, dass der Höhenzuwachs der Flatterulme vergleichbar früh und ähnlich zur Esche kulminiert. Der Höhenzuwachs der Eiche mit ihrer deutlich höheren Lebensdauer gipfelt wesentlich später als bei Flatterulme und Esche. In Ermangelung einer eigenen Ertragstafel für die Flatterulme, würde man daher zumindest im Höhenverlauf eher die Verwendung der Eschen-Ertragstafel unterstellen.
Fazit
Dennoch ist in der Praxis und aus dem gezielten Anbau bisher noch zu wenig zu dieser Art für mitteleuropäische Verhältnisse bekannt. Wichtig ist es daher, die bestehenden und neuen Anbauten der Flatterulme (siehe Abbildung 5) auszuwerten, um für diese relevante, spannende heimische Baumart ökologische, waldbauliche und waldwachstumskundliche Rückschlüsse ziehen zu können.
Danksagung
Zusammenfassung
Ihre große klimatische Amplitude belegt auch ihr weites Verbreitungsgebiet von Nordspanien bis weit nach Russland. Dies verschafft ihr auch in Zukunft eine günstige Perspektive. Eine moderate Erwärmung in Bayern in der Folge des Klimawandels würde ihre derzeitige Verbreitung bezüglich Temperaturgrenzen vermutlich nicht gefährden und ihre Anbaufähigkeit in den mittleren Lagen der Mittelgebirge erheblich ausdehnen. Die Flatterulme zeigt ein rasches Jugendwachstum. Der Alters-Höhenverlauf der Baumart besitzt das Potenzial auf entsprechendem Standort mit dem der Esche verglichen zu werden, bei einer Baumhöhe von 29 m im Alter von 100 Jahren.
- Altherr, E.; Unfried, P.; Hradetzky, J.; Hradetzky, V. (1979): Statistische Rindenbeziehungen als Hilfsmittel zur Ausformung und Aufmessung unentrindeten Stammholzes. – Mitt. Forstl. Versuchs- und Forschungsanstalt Baden-Württemberg 93, 117 S.
- Bayerisches Staatsministerium für Ernährung, Landwirtschaft und Forsten (2018): Hilfstafeln für die Forsteinrichtung. München.
- Brandl, S.; Mette, T.; Falk, W.; Vallet, P.; Rötzer, T.; Pretzsch, H. (2018): Static site indices from different national forest inventories. Harmonization and prediction from site conditions. In: Ann For Sci 75 (2), S. 739. DOI: 10.1007/s13595-018-0737-3.
- Butzke, H. (1969): Über die Böden der feuchten Eichen-Hainbuchenwälder im zentralen Teil des westfälischen Münsterlandes (Kernmünsterland). – Fortschr. Geol. Rheinl. u. Westf. 17: 207-218.
- Caudullo, G.; Welk, E.; San-Miguel-Ayanz, J. (2017): Chorological maps for the main European woody species. Data in Brief (12), S. 662-666. Doi:10.1016/j.dib.2017.05.007
- Collin, E. (2003): EUFORGEN Technical Guidelines for genetic conservation and use for European white elm (Ulmus laevis). International Plant Genetic Resources Institute, Rome, Italy. 6 Seiten.
- Conrad, V. (1946): Usual formulas of continentality and their limits of validity. In: Eos T Am Geophys Un 27 (5), S. 663. DOI: 10.1029/TR027i005p00663.
- Degenhardt, L.M. (2016): Flatterulme zwischen Lech und Isar. – Unveröff. Bachelorarbeit Hochschule Weihenstephan-Triesdorf, Fakultät Wald und Forstwirtschaft, 52 S. + Anh.
- Devetakovic, J.; Stanković, D.; Ivetic, V.; Sijacic/Nikolic, M.; Maksimović, Z. (2016): Potential of different European White Elm (Ulmus laevis Pall.) genotypes for phytoextraction of heavy metals. – Fresenius Environmental Bulletin. 25. 4318-4323.
- Dister, E. (1980): Bemerkungen zur Ökologie und soziologischen Stellung der Auenwälder am nörlichen Oberrhein (Hessische Rheinaue). – Colloques phytosciologiques 9 (Les forets alluviales). – Strasbourg, S. 343-363.
- Ehrendorfer, F. (1978): Geobotanik in: Lehrbuch der Botanik für Hochschulen, begründet von E. Strasburger, F. Noll, H. Schenck, A.F.W. Schimper. 13. Auflage, Stuttgart 1978, S. 979
- Ellenberg, H. et al. (1992): Zeigerwerte von Pflanzen in Mitteleuropa (2. Aufl.). – Scripta Geobotanica (Göttingen) 18, 258 S.
- Ellenberg, H.; Dierschke, H. (2010): Vegetation Mitteleuropas mit den Alpen. In ökologischer, dynamischer und historischer Sicht; 203 Tabellen. Unter Mitarbeit von Christoph Leuschner. 6., vollständig neu bearbeitete und stark erweiterte Auflage. Stuttgart: Verlag Eugen Ulmer (UTB Botanik, Ökologie, Agrarund Forstwissenschaften, Geographie, 8104).
- ETH Zürich (1995): Mitteleuropäische Waldbaumarten. Artbeschreibung und Ökologie unter besonderer Berücksichtigung der Schweiz. Hrsg. Professur für Waldbau und Professur für Forstschutz und Dendrologie, S. 238-243.
- Ewald, J.; Kölling, C. (2009): Wo der Wald an Grenzen stößt. LWF aktuell 71, S. 34-36.
- Fick, S.E.; Hijmans, R.J. (2017): WorldClim 2. New 1-km spatial resolution climate surfaces for global land areas. In: Int. J. Climatol 37 (12), S. 4302-4315. DOI: 10.1002/joc.5086.
- GBIF.org (2019): GBIF Occurrence Download. Ulmus laevis Pall., zuletzt geprüft am 17.04.2019.
- Härdtle, W.; Ewald, J.; Hölzel, N. (2004): Wälder des Tieflandes und der Mittelgebirge. – Stuttgart, 252 S.
- Hempel, G.; Wilhelm, K. (1889): Die Bäume und Sträucher des Waldes in botanischer und forstwirtschaftlicher Beziehung. III. Abteilung. Wien, 140 S.
- Jüttner (1975): Ertragtafel Eiche (1955). In: Reinhard Schober (Hg.): Ertragstafeln der wichtigsten Baumarten. bei verschiedener Durchforstung. Frankfurt M.: J.D. Sauerländer's Verlag, S. 12-25.
- Kempeneers, P.; Sedano, F.; Seebach, L.; Strobl, P.; San-Miguel- Ayanz, J. (2011): Data Fusion of Different Spatial Resolution Remote Sensing Images Applied to Forest-Type Mapping. In: IEEE Transactions on Geoscience and Remote Sensing 49 (12), S. 4977-4986. DOI: 10.1109/TGRS.2011.2158548.
- Kiermeier, P. (1988): Bund Deutscher Baumschulen (BDB)- Handbuch Wildgehölze (2. Aufl.). – Pinneberg, 231 S.
- Köstler, J.N.; Brückner, E.; Bibelriether, H. (1968): Die Wurzeln der Waldbäume. – Hamburg und Berlin, 284 S.
- Kreutzer, K. (1987): Die standörtlichen Verhältnisse im Auwald- Schriftenr. Bayer. Forstverein 7: 64-79.
- Kutschera, L.; Lichtenegger, E. (2013): Wurzelatlas mitteleuropäischer Waldbäume und Sträucher (2. Aufl.). – Graz, 604 S.
- Leuschner, C.; Ellenberg, H. (2017): Ecology of Central European Forests. Vegetation Ecology of Central Europe, Vol. I. – Cham/ Schweiz (Springer), 971 S.
- Li, M.; Lopez, R.; Venturas, M.; Pita, P.; Gordaliza, G.G.; Gil, L.; Rodriguez-Clcerrada, J. (2015): Greater resistance to flooding of seedlings of Ulmus laevis than Ulmus minor is related to the maintenance of a more positive carbon balance, Trees 29: 835-848.
- Linkola, K. (1934): Die Flatterulme in der Gegend des Vanajavesisees. – Acta Forest. Fennica 40: 155.203.
- Macher, C. (2008): Wenn Bäumen des Wasser bis zum Hals steht. Eine bayernweite Umfrage zur Hochwassertoleranz von Waldbäumen. – LWF aktuell 66: 26-29.
- Mayer, H. (1992): Waldbau auf soziologisch-ökologischer Grundlage; 25 Tabellen. 4., teilw. neu bearb. Aufl. Stuttgart: G. Fischer.
- Ministerium für Ländlichen Raum, Ernährung, Landwirtschaft und Forsten Baden-Württemberg (Hg.) (1993): Hilfstabellen für die Forsteinrichtung.
- Müller-Kroehling, S. (2003a): Ulmus laevis PALL. – Flatterulme. – In Weisgerber, H. et al. (Hrsg.): Enzyklopädie der Holzgewächse (33. Ergänzungslieferung).
- Müller-Kroehling, S. (2003b): Flatterulme – ein unbekannter Baum. Zehn verbreitete Irrtümer zu einer heimischen Baumart. – AFZ/Der Wald 25: 1282-1286.
- Müller-Kroehling, S. (2003c): Die Flatterulme in Bayern. – LWF aktuell 42: 51-54.
- Müller-Kroehling, S. (2005): Flatterrüster (Ulmus laevis PALL.) – eine wenig bekannte heimische Holzart. - Holz-Zentralblatt 131 (8): 109-111.
- Müller-Kroehling, S. (2011): Eschentriebsterben, Erlen-Phytophtora: Die Flatterulme als Alternative und Ersatz in geschädigten Feuchtwaldbeständen. – AFZ/Der Wald 19: 36-38.
- Müller-Kroehling, S.; Clauss, V. (2011): Alternative zu Esche und Schwarzerle – ein Plädoyer für die Flatterulme. – Forstinfo 6: 4.
- Osenstetter, S.; Falk, W.; Reger, B.; Beck, J. (2013): Wasser, Luft und Nährstoffe – alles, was ein Baum zum Leben braucht. In: LWF aktuell (94), S. 12-17.
- Pepori, A.L.; Selvaggi, A.; Varese, P.; Ghelardini, L.; Santini, A. (2013): About Ulmus laevis in Italy. - Third In. Elm Conference 2013 (Florence (Italy) 9-11 October 2013), Abstractts, 1 pp.
- Prpic, B., Seletkovic, Z.; Tikvic, I. (2005): Ecological constitution of the tree species in floodplain forests. – In: Akademia Sumarskih
- Rebel, K. (1924): Waldbauliches aus Bayern (Bd. I und II). – Diessen, 239 u. 228 S.
- Roloff, A. (2010): Bäume. Lexikon der praktischen Baumbiologie. 2., völlig neu überarb. Aufl.
- Sauter, R. (2003): Waldgesellschaften in Bayern. – Landsberg, 224 S.
- Schmitz, W. (1992): Die Eichhorst. Erfahrungen mit meinem Wald. – Hamburg, 131 S.
- Schütt, P.; Schuck, H.J.; Stimm, B. (2002): Ulmus laevis Pall. In: Lexikon der Baum- und Straucharten. Sonderausgabe 2002 für Nikol Verlagsgesellschaft mbH & Co. KG, Hamburg, 581 S.
- Seibert, P. (1987): Der Eichen-Ulmen-Auwald (Querco-Ulmetum Issl. 24) in Süddeutschland. - Natur und Landschaft 62(9): 347-352.
- Späth, V. (1988): Zur Hochwassertoleranz von Auwaldbäumen. – Natur und Landschaft 63(7/8): 312-315.
- Taeger, S.; Kölling, C. (2016): Standortinformationssystem BaSIS. AFZ/Der Wald 4/2016, S. 10-13.
- Tangerding, S. (2010): Zu Struktur und Leistung des Waldes in Europa. Ein latitudinaler Vergleich europäischer Wirtschaftsbaumarten auf der Basis von Ertragstafeln. Diplomarbeit. Technische Universität München, Freising. Lehrstuhl für Waldwachstumskunde.
- Thurm, E.; Falk, W. (2019): Standortsansprüche seltener Baumarten: Wie Expertenwissen Artverbreitungsmodelle ergänzt. AFZ/Der Wald 15, S. 32-35.
- Thurm, E.A.; Hernandez, L.; Baltensweiler, A.; Ayan, S.; Rasztovits, E.; Bielak, K.; Zlatanov, T.M.; Hladnik, D.; Balic, B.; Freudenschuss, A.; Büchsenmeister, R.; Falk, W. (2018): Alternative tree species under climate warming in managed European forests. In: Forest Ecol Manag 430, S. 485-497. DOI: 10.1016/j. foreco.2018.08.028.
- Venturas, M.; Fernández, V.; Nadal, P.; Guzmán, P.; Lucena, J.J.; Gil, L. (2014a): Root iron uptake efficiency of Ulmus laevis and U.minor and their distribution in soils of the Iberian Peninsula. – Frontiers of Plant Science 5, article 104, 1-9.
- Venturas, M.; Fuentes-Utrilla, P.; López, R.; Perea, R.; Fernández, V.; Gascó, A., Guzmán, P.; Li, M.; Rodríguez-Calcerrada, J.; Miranda, E.; Domínguez, J.; González-Gordaliza, G.; Zafra, E.; Fajardo- Alcántara, M.; Martín, J.A.; Ennos, R.; Nanos, N.; Lucena, J.J.; Iglesias, S.; Collada, C.; Gil, L. (2014b): Ulmus laevis in the Iberian Peninsula: a review of its ecology and conservation. – iForest- Biogeosciences and Foresty 8: 135-142.
- Venturas, M.; Nanos, N.; Gil, L. (2014c): The reproductive ecology of Ulmus laevis Pallas in a transformed habitat. – Forest Ecology and Management. 312: 170-178.
- Viktorov, D.P.; Bystrjancev, N.I. (1960): Pvysenie zasuhoustojcivosti sejancev berezy i vjaza pod vlijaniem fosfornyh udobrenij (Increasing the drought resistance of Birch and Elm seedlings with P fertilizers). – Lesn. Z., Arhangel’sk 3(3): 35-40 (aus Forestry Abstracts).
- Vyskot, M. (1984): Vliv vodohospodarskych uprav na vyvoj tloust’koveho prirustu drevin luzniho lesa (Effect of water-management practices on the diameter increment of floodplain forest tree species). – Lescnictvi 30(9): 737-765 (aus Forestry Abstracts).
- Walter, H. (1931): Fam. Ulmaceae. – In: Kirchner, O.v., Loew, F. und Schröter, C. (Hrsg.): Lebensgeschichter der Blütenpflanzen Mitteleuropas. Spezielle Ökologie der Blütenpflanzen Deutschlands, Österreichs und der Schweiz. Bd. II, 1. Abt., Bogen 39-41 (Lieferung 38/39). – Stuttgart, 1231 S.
- Wimmenauer (1975): Ertragstafel Esche (1919). In: Reinhard Schober (Hg.): Ertragstafeln der wichtigsten Baumarten. bei verschiedener Durchforstung. Frankfurt M.: J.D. Sauerländer’s Verlag, S. 52-53.
- Znanosti (2005, Hrsg.): Floodplain forests in Croatia, S. 147-167.
Beitrag zum Ausdrucken
Weiterführende Informationen
Autoren
- Eric Andreas Thurm
- Wolfgang Falk
- Stefan Müller-Kroehling


